Obtención del cloruro de magnesio
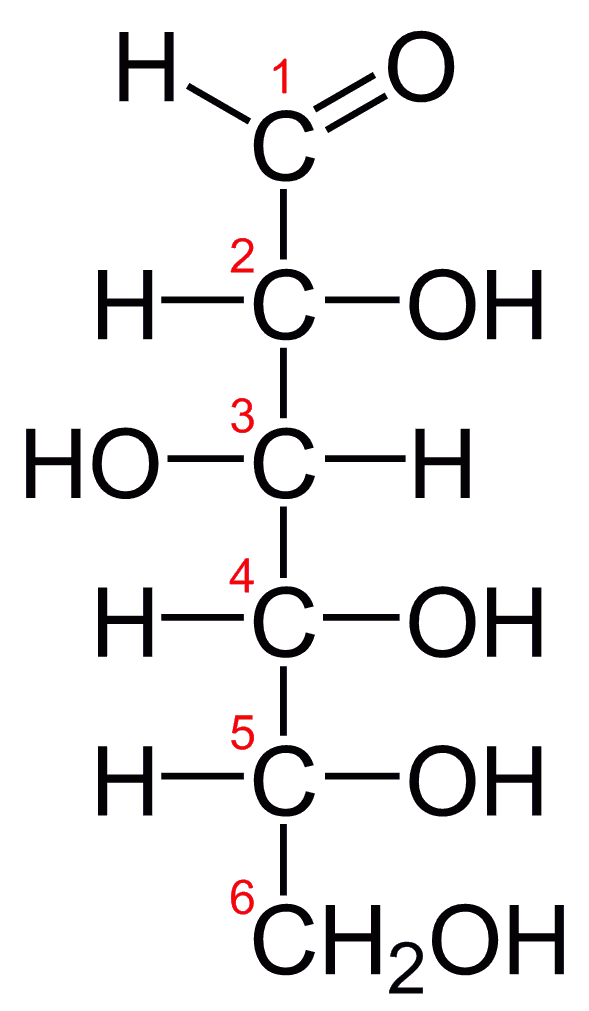
El cloruro de magnesio, de fórmula MgCl2 es un compuesto mineral iónico a base de cloro, cargado negativamente, y magnesio, cargado positivamente. El hexahidrato, cuando se calienta, puede experimentar una hidrólisis parcial. El cloruro de magnesio puede extraerse de salmueras o del agua de mar y es una gran fuente de magnesio, obtenido por electrólisis. El cloruro de magnesio puede presentarse en forma anhidra, bi-hidratado o hexahidratado. Este último compuesto se presenta como cristales romboides de gran belleza ornamental. Es una sal delicuescente (del latín deliquescere, hacerse líquido), por lo que tiene afinidad química por el agua, pudiendo absorber cantidades relativamente altas de agua si se expone a la atmósfera, formando una solución líquida.
Procedimiento
Para este experimento, que es muy sencillo, requieres:
Cinta de magnesio
Solución de HCl 1M (Si no te la dan en la escuela, lleva "ácido muriático" que es comercial, debes tener en tu casa un poco, que está al 5% m/m aprox.)
Procedimiento:
1.- Colocas un trozo pequeño de cinta de magnesio en un tubo de ensaye. Si está un poco "viejo", dale una limadita para que quede el Magnesio bien expuesto.
2.- Agregas 2 mL del HCl que tengas y agitas ligeramente.
Rápidamente, verás que se forman burbujas en el líquido, es el hidrógeno (H2) gaseoso que se está formando. El MgCl2 se queda disuelto en el agua.
Solución de HCl 1M (Si no te la dan en la escuela, lleva "ácido muriático" que es comercial, debes tener en tu casa un poco, que está al 5% m/m aprox.)
Procedimiento:
1.- Colocas un trozo pequeño de cinta de magnesio en un tubo de ensaye. Si está un poco "viejo", dale una limadita para que quede el Magnesio bien expuesto.
2.- Agregas 2 mL del HCl que tengas y agitas ligeramente.
Rápidamente, verás que se forman burbujas en el líquido, es el hidrógeno (H2) gaseoso que se está formando. El MgCl2 se queda disuelto en el agua.
Objetivo
Obtener el cloruro de magnesio de forma segura
PIPETEO
Técnica del pipeteo
La técnica del pipeteo abarca diferentes herramientas y medios que se requieren para pipetear. El empleo de la técnica del pipeteo permite dosificar líquidos de forma rápida y precisa. Las herramientas utilizadas para ello se denominan pipetas. Debido a la elevada importancia de la técnica del pipeteo en laboratorios de cualquier tipo, desde la medicina hasta la química, a lo largo de los años se han desarrollado diferentes pipetas de múltiples tamaños y versiones. La versión más conocida es la pipeta de medición, se compone de un tubito de vidrio con una escala de volumen grabada, que se estrecha en la punta y lleva el otro extremo o bien abierto, o bien cerrado con una pera de succión. Con esta pipeta se pueden absorber cantidades variables de líquidos, de modo que ofrece una alta flexibilidad y puede así aplicarse en múltiples ámbitos. La desventaja de esta pipeta es sin embargo la imprecisión que conlleva esta flexibilidad. Si hay que conseguir una precisión muy alta en la dosificación, el empleo de una pipeta aforada es imprescindible. Una pipeta aforada no tiene escala de volumen, sino una sola marca para un volumen definido. Otros instrumentos de la técnica del pipeteo son por ejemplo la pipeta Pasteur, la micropipeta, la pipeta multicanal y diversas versiones especiales como la pipeta desechable de plástico. Éstas se emplean sobre todo en la medicina. Se suelen utilizar para tareas de dosificación con exigencias bajas de precisión, como por ejemplo la dosis de colirio.
OBTENCION DE ALCOHOLES
Mencionaremos en este espacio algunos métodos de obtención de alcoholes primarios como asi también las reacciones más importantes que producen.
Reducción de aldehídos: Los aldehídos con hidrógeno y en presencia de un catalizador como el níquel forman alcoholes primarios.
Por reducción de ácidos:
A través del reactivo de Grignard:
El reactivo es el ioduro
de alquil magnesio.
Uno de los metodos que vimos en clase fue el de destilacion, este metodo es muy sencillo es basicamente un proceso por el que la sustancia volátil de una mezcla se separa de otra que no lo es mediante evaporación y posterior condensación de la misma.


http://www.pce-iberica.es/instrumentos-de-medida/instrumentos-laboratorios/tecnica-pipeteo.htm
http://www.quimicayalgomas.com/quimica-organica/alcoholes-aldehidos-cetonas/alcoholes-parte-2/
Escobar.J(2010) "Revisión científica sobre las propiedades del magnesio"
https://www.google.com.co/url?sa=t&source=web&rct=j&url=http://www.asonatura.com/files/REVISION%2520CIENTIFICA%2520SOBRE%2520LAS%2520PROPIEDADES%2520DEL%2520MAGNESIo.pdf&ved=0ahUKEwix-KjRiJnQAhXGwiYKHfPJB_0QFgg_MAQ&usg=AFQjCNFRCL9uYrwsg4AR3Ou2Oc3Re48rKw&sig2=AV0ipipbhMwhJCFdTuIVLQ